| Umsiedlung einer Population des Hirschzungenfarns (Asplenium scolopendrium L.) aus einem Steinbruch in eine Doline des südharzer Gipskarstes von THOMAS BECKER & UTE BECKER
Zusammenfassung
Im Gipskarst des südlichen Harzrandes wurde eine Population des Hirschzungenfarns (Asplenium scolopendrium), die durch Gipsabbau zerstört worden wäre, in eine Doline umgesiedelt und das Schicksal der Pflanzen wurde zehn Jahre lang verfolgt. 90 % der umgesiedelten Pflanzen überlebten in dieser Zeit. Im dritten Jahr nach der Umsiedlung traten erste Jungpflanzen auf. Nach zehn Jahren zählten wir 1.110 Nachkommen, von denen 171 reproduzierten. Die Anzahl adulter Pflanzen nahm damit um 378 % zu. Die gesamte Population (adulte und juvenile Pflanzen) wuchs um 1.781 %. Pflanzen, die in einen Felshang und eine Blockhalde mit Feinboden gepflanzt worden waren, wuchsen besser als solche in einer Felswand ohne Feinboden. Allerdings konnten sich in der Felswand, wo sich im Herbst keine Laubdecke bildet, mehr Jungpflanzen etablieren als auf dem Felshang, wo im Herbst eine dicke Laubdecke liegt. Obwohl die Umsiedlung der Hirschzungenpopulation erfolgreich war, stellt die Maßnahme keinen Ersatz für die Zerstörung der natürlichen Wuchsorte der Art durch Gipsabbau dar. Der Schutz der natürlichen Wuchsorte muss Vorrang haben. Abstract
Transplantation of a population of the hart’s tongue fern (Asplenium scolopendrium L.) from a quarry into a dolina in the gypsum karst of the southern Harz Mts. In the gypsum karst at the southern edge of the Harz Mountains, parts of a population of the hart’s tongue fern (Asplenium scolopendrium) which would have been destroyed by a quarry were transplanted into a dolina and the fate of the plants was recorded over ten years. 90 % of the plants survived over this time. First progenies were recorded in the third year after transplantation of mother plants. In the tenth year after transplantation 1,110 progenies were recorded, 171 of them reproducing. Thus the number of adult plant increased by 378 % and the overall population by 1,781 % after ten years. Plants which were planted at a rocky slope and a boulder heap where soil was available grew better than plants in crags without soil. In contrast, more juveniles established in the crags, where no fallen leaves were accumulated. We conclude that transplantations are a suitable measure in order to preserve hart’s tongue fern populations. However, such measurements cannot compensate ongoing destruction of natural habitats by gypsum mining activities at the southern edge of the Harz Mountains. The conservation of natural populations must be prior to transplantations. Résumé
Dans le karst gypseux du sud du Harz, une population de fougères scolopendres (Asplenium scolopendrium) menacée par l’extension d’une carrière de gypse a été transplantée dans une doline et suivie pendant 10 ans. 90 % des individus déplacés ont survécu durant cette période et les premières nouvelles plantules sont apparues trois ans après le transfert. Au bout de 10 ans, nous avons dénombré 1 110 nouveaux pieds dont 171 se sont reproduits. La population réimplantée a donc augmenté de 378 % pour les pieds adultes et de 1 781 % au total (adultes et juvéniles). Les individus replantés sur des versants rocheux ou ébouleux avec un sol fin ont manifesté une croissance plus importante que ceux installés sur une paroi rocheuse dépourvue de sol fin. Davantage de plantules se sont toutefois établies sur la paroi rocheuse dépourvue de litière automnale que sur la pente où les feuilles mortes s’accumulaient. Bien que le déplacement de cette population de fougères langue de cerf ait été un succès, cette mesure ne constitue pas une compensation à la destruction des habitats naturels de cette espèce par l’exploitation du gypse et la protection des habitats naturels devrait constituer une priorité. Einleitung
Ansiedlungen von Pflanzenpopulationen sind ein Kernstück der „Global Strategy for Plant Conservation“ und leisten einen Beitrag zur Umsetzung der „Convention on Biodiversity“ von Rio de Janeiro aus dem Jahre 1992 (UNITED NATIONS 1993). Sie können verschiedenen Zielen dienen: Erstens kann die Biodiversität degradierter Lebensräume wiederhergestellt werden (z. B. HÖLZEL et al. 2002 für Stromtalwiesen, KIEHL et al. 2006 für Kalkmagerrasen, MOTTL et al. 2006 für Wälder). Zweitens kann durch Einführung von Schlüsselarten ein bestimmtes Ökosystem (wieder-)hergestellt werden, z. B. durch Wiedereinführung von Calluna vulgaris in degenerierte Heidelandschaften (MITCHELL et al. 2008) oder durch Etablierung von Sphagnum-Arten zur Wiederherstellung von Mooren (GRAF & ROCHEFORT 2008). Drittens können aus Artenschutzgründen seltene oder in einem Gebiet ausgestorbene Arten (wieder-)eingeführt werden, wie z. B. Wilder Wein (Vitis vinifera subsp. silvestris) im Rheintal (ARNOLD et al. 2005), die Finger-Küchenschelle (Pulsatilla patens) in der Münchner Schotterebene (RÖDER & KIEHL 2008) oder Gladiolus imbricatus in Auenlandschaften in Estland (JOGAR & MOORA 2008). Artenschutzgründe sind auch ein Motiv für die Umsiedlung unmittelbar bedrohter Populationen. Solche Umsiedlungen sind bei Tieren verbreitet – man denke nur an die Umsiedlung flugunfähiger neuseeländischer Vögel auf Inseln ohne unnatürliche Feinde (ELLIOTT et al. 2001). Pflanzenpopulationen wurden dagegen bisher kaum umgesiedelt. 
Abb. 1: (A) Neues Habitat der Hirschzungenpopulation in der Doline am Blossenberg und (B) ehemaliges Habitat am Lichtenstein. Die gelben Pfeile zeigen die Lage der Pflanzgruppen und die schwarzen Pfeile den ehemaligen Wuchsort der Population an. Fotos: A) T. Becker 15.10.2005, B) G. Ellwanger 1999. Gezielte Ansiedlungen von Pflanzenpopulationen müssen nicht immer erfolgreich sein (ARNOLD et al. 2005), sind es aber bei fachkundiger Durchführung in vielen Fällen (z. B. HÖLZEL & OTTE 2003, EBEL 2006, MASCHINSKI & DUQUESNEL 2006).
Mitunter entwickeln sich gezielt angesiedelte Populationen sogar besser als bestehende (z. B. COLAS et al. 2008) oder zumindest gleichwertig (z.B. MORGAN 2000, MARRERO-GÓMEZ 2007). Die meisten Studien messen jedoch nur den kurzfristigen Erfolg sol- cher Maßnahmen, während Studien, die den dauerhaften Erfolg untersuchen, selten sind (z. B. BOTTIN et al. 2007, COLAS et al. 2008).
Vorliegende Studie beschreibt die Umsiedlung einer Population des Hirschzungenfarns (Asplenium scolopendrium L., Synonym Phyllitis scolopendrium (L.) Newm.) am südwestlichen Harzrand bei Osterode aus einem Steinbruch in eine Doline, um dadurch die Population vor der Zerstörung zu retten. Die Hirschzunge gilt in Niedersachsen als „gefährdet“ und ist nach der Bundesartenschutzverordnung „besonders geschützt“ (KORNECK et al. 1996, GARVE 2007). Ebenfalls besonders geschützt war bereits zum Zeitpunkt seiner Zerstörung der betreffende Schluchtwald, der nach der Fauna-Flora-Habitat-Richtlinie vom 21.5.1992 einen „prioritären Lebensraumtyp“ (Natura 2000-Code *9180) bildet (EUROPEAN UNION 1992, SSYMANK et al. 1998). Dennoch und trotz spektakulärer Protestaktionen der damaligen „Initiative Naturschutzstudium an der Universität Göttingen“ und der Naturfreunde Göttingen e.V. in Goslar sowie vor dem Niedersächsischen Landtag weitete die Firma HeidelbergCement AG 1997 ihren Gipstagebau am Lichtenstein in Schluchtwälder mit u.a. der betreffenden Hirschzungenpopulation aus. Im Herbst 1997, kurz bevor der Abbau die Hirschzungenpopulation erreicht hätte, entschlossen wir uns für eine Umsiedlung der verbliebenen Pflanzen in eine knapp 4 km entfernte Doline am Blossenberg südlich von Osterode. Diese Doline war von der Hirschzunge nicht besiedelt, erschien uns jedoch als mögliches Habitat für die Art geeignet. Das Wachstum der umgesiedelten Pflanzen sowie die Entwicklung der Population wurde zehn Jahre lang untersucht. Die Ergebnisse der Untersuchung werden hier vorgestellt. Material und Methoden
Im September 1997 wurden aus der betreffenden Hirschzungenpopulation am Lichtenstein 59 adulte Pflanzen entnommen und im Neuen Botanischen Garten Göttingen kultiviert. Im März 1999 wurden die Pflanzen in eine südlich von Osterode gelegene Doline ausgepflanzt (Abb. 1, 2; genaue Ortsangaben in BECKER & BECKER 2010). Wir pflanzten die Hirschzungen in sechs Gruppen (im Folgenden als „Pflanzgruppen“ bezeichnet) mit je 7-12 Individuen in die Felswände, auf einen Sims, einen Felshang und eine Blockhalde am Grund der Doline (die letzten drei Habitate werden hier als „Nicht-Felswandhabitate“ zusammengefasst). Die Doline hat einen Durchmesser von ca. 40 m und ist ca. 10 m tief. Um sie herum wächst ein Rotbuchenwald und in ihr ein Schluchtwald mit Acer pseudoplatanus und Ulmus glabra. In den letzten zehn Jahren sind in der Doline wiederholt ältere Bäume abgerutscht und zusammengebrochen, wodurch das Kronendach immer lückig war (Abb. 3). Die üppig entwickelte Bodenvegetation besteht aus Farnen (Athyrium filix-femina, Dryopteris filixmas, D. dilatata, Polystichum aculeatum, Asplenium trichomanes, Cystopteris fragilis), Kräutern (Impatiens nolitangere, Geranium robertianum), Stauden (Urtica dioica) und zahlreichen Moosen. 
Abb. 2: Üppig entwickelter Hirschzungenfarn zehn Jahre nach seiner Umsiedlung; Foto: T. Becker 31.10.2009 Das Schicksal der Pflanzen (tot oder lebendig), die Anzahl Blätter, die Länge des längsten Blattes und die Produktion von Sporen (ja/nein) wurden pro umgesiedelte Pflanze zuerst jährlich und später alle zwei Jahre im Spätsommer oder Frühherbst aufgenommen (BECKER & BECKER 2010). Bei jeder Aufnahme wurde zudem die Anzahl der produzierten Jungpflanzen gezählt (Abb. 4). Um das Ausbreitungspotential der Art einzuschätzen, wurde 2009 der Abstand der Jungpflanzen zur nächsten (mutmaßlichen) Mutterpflanze gemessen. Zusätzlich wurde bei 265 Jungpflanzen die Länge des längsten Blattes gemessen.
Um Pseudoreplikation zu vermeiden, wurden alle gemessenen Werte vor den statistischen Analysen über die Pflanzgruppen gemittelt. Zusammenhänge zwischen den Wachstumsvariablen und der Zeit wurden mit einfacher Varianzanalyse mit Messwiederholung, und Unterschiede in der Variation der Größe der Jungpflanzen zwischen den sechs Pflanzgruppen mit einfacher Varianzanalyse untersucht. Die relative Wachstumsrate (RWR) der umgesiedelten Pflanzen wurde wie folgt berechnet: RWR = (Größe der Pflanzen 2009 – Größe der Pflanzen 2000) / Größe der Pflanzen 2000 x 100, wobei die „Größe der Pflanzen“ jeweils aus der Anzahl Blätter x der Länge des längsten Blattes gebildet wurde. Unterschiede in der RWR der Pflanzen aus Felswand- und Nicht-Felswandhabitaten wurden mit einfacher Varianzanalyse mit Messwiederholung untersucht. Alle statistischen Analysen wurden mit dem Programm SPSS (SPSS Inc. 2006) durchgeführt. 
Abb. 3: Vermessung der umgesiedelten Hirschzungen in der Doline. Unten links befindet sich ein kleines Schluckloch, wo ständig Gips gelöst und abgeführt wird, was zu einem ständigen Absacken des Bodens führt, sodass die darüber liegende Felswand dauerhaft steil bleibt. Zahlreiche umgestürzte Bäume lassen die starke Dynamik des Lebensraumes erkennen. Foto: T. Becker 19.9.2009.  Abb. 4: „Von selbst“ angesiedelte Nachkommen der Hirschzunge in einer Felswand; Foto: T. Becker 31.10.2009 Ergebnisse
Schicksal und Wachstum der umgesiedelten Pflanzen
52 der 59 umgesiedelten Pflanzen (88 %) überlebten den Untersuchungszeitraum von zehn Jahren. Sieben Pflanzen (12 %) starben in dieser Zeit durch Absturz aus der Felswand (drei Pflanzen), Überschüttung mit Herbstlaub (eine Pflanze) oder ohne erkennbaren Grund (drei Pflanzen). Die Anzahl der Blätter pro Pflanze nahm signifikant von durchschnittlich zehn im Jahr der Umsiedlung auf 26 nach zehn Jahren zu (Abb. 5A). Gleichzeitig nahm der Schwankungsbereich der Anzahl der Blätter zwischen den Pflanzengruppen mit der Zeit signifikant zu (Fehlerbalken in Abb. 5A; df = 5, F = 31,3, P = 0,003, r² = 0,94, P < 0,001).
Die Länge des längsten Blattes pro Pflanze verdoppelte sich von ca. 25 cm im ersten auf 50 cm im zehnten Jahr (Abb. 5B). Die Größe der Pflanzen der Nicht-Felswandhabitate nahm während der 10 Jahre um 679 % zu, während Pflanzen, die in die Felswände gepflanzt wurden, um nur 395 % größer wurden. Populationsdynamik
Bereits ein Jahr nach dem Auspflanzen bildeten 68 % der Pflanzen Sporen. Drei Jahre später, im vierten Jahr nach der Umsiedlung, sporolierten fast alle Pflanzen (Abb. 6A). Im dritten Jahr der Umsiedlung traten die ersten Jungpflanzen auf. Die Anzahl der Jungpflanzen stieg zunächst langsam und dann immer schneller auf schließlich 1.110 im zehnten Jahr an (Abb. 6B). Im Durchschnitt hatte jede umgesiedelte Hirschzunge 19 Nachkommen. Insgesamt nahm in den zehn Jahren die Anzahl der adulten Pflanzen um 378 % zu. Die gesamte Population (adulte und juvenile Pflanzen) wuchs um 1.781 %.
Einfluss des Mikrohabitats auf die Vermehrung und das Wachstum der Jungpflanzen und Mutterpflanzen, die in den Felswänden wuchsen, hatten nach zehn Jahren durchschnittlich 25 Nachkommen gebildet, während Mutterpflanzen, die in den Nicht-Felswandhabitaten (Felshang, Felssims, Blockhalde) wuchsen, im Durchschnitt nur neun Nachkommen hatten (n = 6, F = 1,71, P < 0,261). Allerdings hatten die Nachkommen in den Nicht-Felswandhabitaten viermal so lange Blätter wie die in den Felswänden (15,4 cm vs. 3,9 cm; n = 264 Nachkommen, F = 49,5, P < 0,001). Diskussion
Unsere Studie zeigt, dass die betreffende Doline als Lebensraum für die Hirschzunge geeignet ist. Damit stellt sich die Frage, warum sie nicht auf natürlichem Wege besiedelt wurde, zumal die nächsten Hirschzungenpopulationen als mögliche Lieferanten von Diasporen kaum vier Kilometer entfernt wachsen und die leichten Sporen vermutlich gut fliegen können. Der wichtigste Grund für die ausgebliebene Besiedlung ist vermutlich die Seltenheit der Art im Gebiet bzw. die dadurch bedingte geringe Sporenmenge – mit anderen Worten: Die Art kann im Gebiet keinen hohen Ausbreitungsdruck aufbauen, daher gelangen zu selten Sporen in unbesiedelte Habitate. Die Seltenheit der Art am südlichen Harzrand kann wiederum durch die Seltenheit geeigneter Habitate erklärt werden: Die Hirschzunge ist an luftfeuchte Felsstandorte gebunden (OBERDORFER 2001) und gilt gegenüber Trockenheit als empfindlich (KELSALL et al. 2004). Zudem können am südlichen Harzrand, der am nordöstlichen Arealrand der Art liegt, trockene Sommer und kalte Winter die frostempfindliche Hirschzunge einschränken. Nach KAPPEN (1964) bzw. LÖSCH et al. (2007) erträgt die Art bis -14 °C bzw. -19 °C Frost.
Ein weiterer Grund für die ausgebliebene Besiedlung der Doline könnte sein, dass die meisten Sporen nicht sehr weit fliegen, wie die in unserer Studie festgestellten geringen Distanzen zwischen Jungpflanzen und Mutterpflanzen zeigen. Allerdings hatten sich einige Jungpflanzen außerhalb der Doline und oberhalb von Mutterpflanzen angesiedelt, was auf Windausbreitung und damit die grundsätzliche Möglichkeit von Fernausbreitung hindeutet. Dies gilt auch für synanthrope Vorkommen an Mauern und Brunnenschächten in Städten (SEBALD et al. 1993; pers. Beob.). In jedem Fall gibt es am südlichen Harzrand durchaus noch luftfeuchte Felshabite, die als Lebensraum für die Hirschzunge geeignet erscheinen, jedoch nicht besiedelt sind. Vermutlich wären hier weitere Ansiedlungen möglich.
Die mit der Zeit zwischen den sechs Pflanzgruppen zunehmend unterschiedlichen Blattzahlen können durch unterschiedliche Nährstoff- und auch Lichtversorgung erklärt werden. So waren in den Felswänden (Pflanzgruppen 1 und 2) die Pflanzen wegen schlechterer Nährstoffversorgung und weniger Licht deutlich kleiner. Die stärkere Vermehrung der Art in den Felswänden zeigt dagegen, dass die Keim- und Etablierungsbedingungen hier besser sind, da es hier viel offenen Fels und Mineralboden gibt und sich im Herbst keine Laubschicht ausbildet. Auf dem Felshang und den größeren Felssimsen werden die Jungpflanzen dagegen im Herbst mit Buchenlaub überschüttet, was zu erheblicher Mortalität führen dürfte; auf den Laubdecken siedeln sich erst gar keine Pflanzen an. Auch FLINN (2007) betont die Bedeutung von offenem Boden für die Etablierung nordamerikanischer Farne. SCHWARZBERG (2008) postuliert gleiches für den Wiederansiedlungserfolg von Pinguicula vulgaris in Felswänden im thüringischen Gipskarst.
In den Felswänden kann dagegen eine dichtwüchsige und relativ große Lebermoosart (Conocephalum conicum) einen negativen Effekt auf die Ansiedlung von Jungpflanzen der Hirschzunge haben. Vermutlich werden diese von dem Lebermoos überwachsen bzw. können auf den Moos-Thalli gar nicht erst keimen. Dafür spricht, dass an einem Wurzelteller einer umgestürzten größeren Buche (Abb. 1, Bildmitte), der viel offenen Boden aber keine Moosrasen aufwies, bereits nach kurzer Zeit viele Jungpflanzen wuchsen, obwohl dieser Wurzelteller von den nächsten Mutterpflanzen relativ weit entfernt war. Ein besonders gutes Mikrohabitat stellt offenbar auch die Blockhalde am Grund der Doline dar. Die Gipsblöcke haben freien Fels und damit gute Ansiedlungsbedingungen an den Rändern, während Bodenansammlungen zwischen und auf den Blöcken später Nährstoffe liefern. Außerdem sammelt sich auf der Blockhalde im Zentrum der Doline weniger schwer zersetzbares Buchenlaub an, da hier u.a. Berg-Ahorn und Berg-Ulme wachsen, deren Laub sich viel schneller zersetzt. Jedenfalls gab es in der Blockhalde nicht nur besonders viele, sondern auch auffällige große Nachkommen mit vielen Sporen. 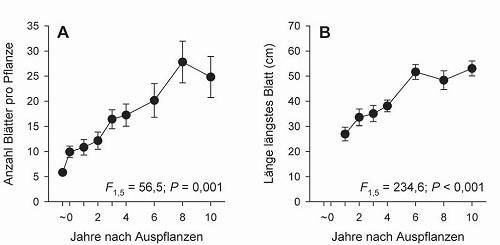
Abb. 5: Entwicklung der (A) Anzahl der Blätter und (B) Länge der längsten Blattes pro umgesiedelte Hirschzungenpflanze über den Zeitraum von zehn Jahren. Dargestellt sind Mittelwerte und + 1 Standardfehler. ~0: Pflanzdatum (März 1999). Die statistischen Kennwerte beziehen sich auf eine Varianzanalyse mit Messwiederholung. 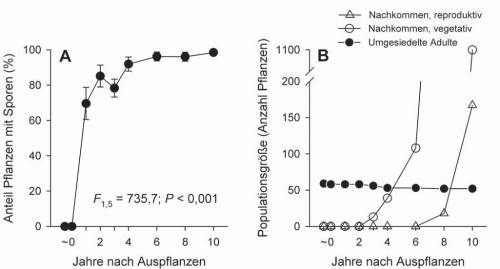 Abb. 6: (A) Anteil der umgesiedelten Hirschzungenpflanzen mit Sporen und (B) die Entwicklung der Hirschzungenpopulation über den Zeitraum von zehn Jahren. In A) sind Mittelwerte und + 1 Standardfehler dargestellt und in B) absolute Werte. ~0: Pflanzdatum (März 1999). Die statistischen Kennwerte in A) beziehen sich auf eine Varianzanalyse mit Messwiederholung. Obwohl „unsere“ Hirschzungenpopulation durch die Umsiedlung vor der Zerstörung gerettet wurde, stellt unsere Maßnahme keinen Ersatz für den Verlust der natürlichen Habitate der Art dar. Lebensraumschutz für die Hirschzunge im südharzer Gipskarst ist nur dann möglich, wenn für die betreffenden Gebiete keine neuen Abbaugenehmigungen erteilt werden bzw. bestehende Genehmigungen und Abbauten gestoppt werden können. Immerhin ist vorläufig sichergestellt, dass keine neuen Abbaugenehmigungen im betreffenden Gipskarst bei Osterode erteilt werden, da 2004 eine 10,88 km² große Fläche der Karstlandschaft südlich von Osterode mitsamt „unserer“ Doline von der EU als FFH-Gebiet „Gipskarstgebiet bei Osterode“ ausgewiesen wurde (ELLWANGER 1999a,b). Allerdings hat das Schutzgebiet im Bereich bestehender und geplanter Steinbrüche (Lichtenstein, Kreuzstiege) fensterartige Aussparungen, von denen zwei ca. 8 ha bzw. 6 ha große nur 150 m bzw. 450 m von „unserer“ Doline entfernt liegen (Karte des NIEDERSÄCHSISCHEN MINISTERIUMS FÜR UMWELT UND KLIMASCHUTZ 2009). Langfristig bleibt nur zu hoffen, dass Gipsprodukte wie Rigips-Platten nicht mehr aus Natur-, sondern REA-Gips hergestellt oder durch andere Produkte ersetzt werden und bis dahin die Verbraucher auf den Kauf von Naturgipsprodukten verzichten. REA-Gips fällt in der Rauchgaswäsche in großen Mengen an und ist mittlerweile so rein, dass er problemlos als Baumaterial eingesetzt werden kann (WIKIPEDIA 2010). Noch hat die Verwendung von Naturgips für die Firmen finanzielle Vorteile, wie in jüngerer Zeit getätigte Ankäufe von thüringischen Gipslagerstätten (darunter auch Naturschutzgebiete) und neue Abbauanträge sogar in FFH- Gebieten deutlich machen. Die einzigartige Gipskarstlandschaft am südlichen Harzrand bleibt somit vorerst durch Abbau von Rohstoffen weiter bedroht. Dank
Wir danken Ursula Schäfer und Götz Ellwanger für Informationen sowie ein Foto, Claudia Giesbert für Hilfe beim Auspflanzen der Hirschzungen, Katharina Schumann für die Übersetzung der französischen Zusammenfassung und Dr. Friedhart Knolle für die Einladung zu dieser Publikation. Der Gesellschaft zur Förderung des Biosphärenreservates Südharz e.V. (www.gipskarst.de) gilt unser Dank für ihr Engagement für den Gipskarst. Literatur | ARNOLD, C., SCHNITZLER, A., DOUARD, A., PETER, R. & GILLET, F. (2005): Is there a future for wild grapevine (Vitis vinifera subsp. silvestris) in the Rhine Valley? – Biodivers. Conserv. 14: 1507-1523 | | BECKER, T. & BECKER, U. (2010): Successful transplantation of a hart’s tongue fern population (Asplenium scolopendrium L.) with ten years of monitoring. – Tuexenia 30: 47-58 | | BOTTIN, L., LE CADRE, S., QUILICHINI, A., BARDIN, P., MORET, J. & MACHON, N. (2007): Re-establishment trials in endangered plants: a review and the example of Arenaria grandiflora, a species on the brink of extinction in the Parisian region (France). – Ecoscience 14: 410-419 | | COLAS, B., KIRCHNER, F., RIBA, M., OLIVIERI, I., MIGNOT, A., IMBERT, E., BELTRAME, C., CARBONELL, D. & FRÉVILLE, H. (2008): Restoration demography: a 10-year demographic comparison between introduced and natural populations of endemic Centaurea corymbosa (Asteraceae). – J. Appl. Ecol. 45: 1468-1476 | | EBEL, F. (2006): Vom Aussterben gerettet: Gips-Fettkraut (gipsbewohnende Sippe von Pinguicula vulgaris L.) – Natursch. Land Sachsen-Anhalt 43: 41-43 | | ELLIOTT, G. P., MERTON, D. V. & JANSEN, P. W. (2001): Intensive management of a critically endangered species: the kakapo. – Biol. Conserv. 99: 121-133 | | ELLWANGER, G. (1999a): Zur Bedeutung des vorgeschlagenen FFH- Gebietes „Gipskarstgebiet bei Osterode“ für das europäische Schutzgebietssystem Natura 2000. – Göttinger Naturkundl. Schr. 5: 169-178 | | ELLWANGER, G. (1999b): Verpflichtung zur Durchführung und Umfang der FFH-Verträglichkeitsprüfung am Beispiel des Rohstoffabbaus im „Gipskarst bei Osterode“. – Natur Landsch. 74: 478- 484 | | EUROPEAN UNION (1992): Council directive 92/43/EEC of 21 May 1992 on the conservation of natural habitats and of wild fauna and flora. – http://eur-lex.europa.eu (Zugriff: 8.8.2010) | | FLINN, K. M. (2007): Microsite-limited recruitment controls fern colonization of post-agricultural forests. – Ecology 88: 3103- 3114 | | GARVE, E. (2007): Verbreitungsatlas der Farn- und Blütenpflanzen in Niedersachsen und Bremen. – Naturschutz Landschaftspfl. Niedersachsen 43: 1-507 | | GRAF, M. D. & ROCHEFORT, L. (2010): Moss regeneration for fen restoration: field and greenhouse experiments. – Restor. Ecol. 18: 121-130 | | HÖLZEL, N., DONATH, T. W., BISSELS, S. & OTTE, A. (2002): Auengrünlandrenaturierung am hessischen Oberrhein – Defizite und Erfolge nach 15 Jahren Laufzeit. – Schriftenr. Vegetationskd. 36: 131-137 | | HÖLZEL, N. & OTTE, A. (2003): Restoration of a species-rich flood meadow by topsoil removal and diaspore transfer with plant litter. – Appl. Veg. Sci. 6: 131-140 | | JOGAR, Ü. & MOORA, M. (2008): Reintroduction of a rare plant (Gladiolus imbricatus) population to a river floodplain – How important is meadow management? – Restor. Ecol. 16: 382-385 | | KAPPEN, L. (1964): Untersuchungen über den Jahresverlauf der Frost-, Hitze- und Austrocknungsresistenz von Sporophyten einheimischer Polypodiaceen (Filicinae). – Flora 155: 123-166 | | KELSALL, N., HAZARD, C. & LEOPOLD, D. J. (2004): Influence of climate factors on demographic changes in the New York populations of the federally-listed Phyllitis scolopendrium (L.) Newm. var. americana. – J. Torrey Bot. Soc. 131: 161-168 | | KIEHL, K., THORMANN, A. & PFADENHAUER, J. (2006): Evaluation of initial restoration measures during the restoration of calcareous grasslands on former arable fields. – Restor. Ecol. 14: 148-156 | | KORNECK, D., SCHNITTLER, M. & VOLLMER, I. (1996): Rote Liste der Farn- und Blütenpflanzen (Pteridophyta et Spermatophyta) Deutschlands. – Schriftenr. Vegetationskd. 28: 21-187 | | LÖSCH, R., BIRON, U., PATRIAS, T. & HÖPTNER, B. (2007): Gas exchange and water relations of Asplenium ferns growing on limestone rocks. – Nova Hedwigia 131: 221-236 | | MARRERO-GOMEZ, M. V., OOSTERMEIJER, J. G. B., CARQUÉ-ÁLAMO, E. & BANARES-BAUDET, A. (2007): Population viability of the narrow endemic Helianthemum juliae (Cistaceae) in relation to climate variability. – Biol. Conserv. 136: 552-562 | | MASCHINSKI, J. & DUQUESNEL, J. (2006): Successful reintroductions of the endangered long-lived Sargent’s cherry palm, Pseudophoenix sargentii, in the Florida Keys. – Biol. Conserv. 134: 122-129 | | MITCHELL, R. J., ROSE, R. J. & PALMER, S. C. F. (2008): Restoration of Calluna vulgaris on grass-dominated moorlands: The importance of disturbance, grazing and seeding. – Biol. Conserv. 141: 2100- 2111 | | MORGAN, J. W. (2000): Reproductive success in reestablished versus natural populations of a threatened grassland daisy (Rutidosis leptorrhynchoides). – Conserv. Biol. 14: 780-785 | | MOTTL, L. M., MABRY, C. M. & FARRAR, D. M. (2006): Seven-year survival of perennial herbaceous transplants in temperate woodland restoration. – Restor. Ecol. 14: 330-338 | | NIEDERSÄCHSISCHES MINISTERIUM FÜR UMWELT UND KLIMASCHUTZ (2009): www.umweltkarten.niedersachsen.de/natura/ (Zugriff: 7.11.2009) | | OBERDORFER, E. (2001): Pflanzensoziologische Exkursionsflora, 8. Aufl. – Ulmer, Stuttgart | | RÖDER, N. & KIEHL, K. (2008): Vergleich des Zustandes junger und historisch alter Populationen von Pulsatilla patens (L.) Mill. in der Münchner Schotterebene. – Tuexenia 28: 121-132 | | SCHWARZBERG, B. (2008): Artenhilfsmaßnahme für die „Gipsrasse“ des Echten Fettkrautes im NSG „Alter Stolberg“ (Landkreis Nordhausen). – Landschaftspfl. Natursch. Thüringen 45: 62-67 | | SEBALD, O., SEYBOLD, S. & PHILIPPI, G. (1993): Die Farn- und Blütenpflanzen Baden-Württembergs. Bd. 1, 2. Aufl. – Ulmer, Stuttgart | | SPSS Inc. (2006): SPSS 15.0 for Windows and Smart-Viewer. SPSS, Chicago, IL, USA | | SSYMANK, A., HAUKE, U., RÜCKRIEM, C. & SCHRÖDER, E. (1998): Das Europäische Schutzgebietssystem NATURA 2000. – Schriftenr. Landschaftspfl. Natursch. 53: 1-560 | | UNITED NATIONS (1993): Convention on biological diversity (with annexes). Concluded at Rio de Janeiro on 5 June 1992. – United Nations Treaty Series 1760 (I-30619): 1-83 | | WIKIPEDIA (2010): de.wikipedia.org/wiki/REA-Gips (Zugriff: 8.8.2010) |
Anschrift der Autoren: Dr. Thomas Becker, Universität Göttingen, Albrecht von Haller-Institut für Pflanzenwissenschaften, Abteilung Pflanzenökologie & Ökosystemforschung, Untere Karspüle 2, 37073 Göttingen, tbecker@gwdg.de; Dr. Ute Becker, Grüne Schule des Botanischen Gartens der Universität Mainz, Anselm Franz von Bentzel-Weg 9b, 55099 Mainz, beckeru@uni-mainz.de
Wir danken der Schriftleitung der Mitteilungen des Verbandes deutscher Höhlen- und Karstforscher für die freundliche Genehmigung, diesen Beitrag ebenfalls veröffentlichen zu dürfen. Weiterer Nachdruck oder Veröffentlichung bzw. Verbreitung in anderen elektronischen Medien nur mit schriftlicher Genehmigung der Schriftleitung. |





